[vc_row][vc_column][vc_column_text]
- Maturalne Układy Okresowe nie zawierają wartości liczb masowych (A). Nie ma ich również w Układach Okresowych z podręczników szkolnych (poziom szkoły średniej). Istnieją wyspecjalizowane Układy Okresowe, które zawierają te liczby masowe (bardziej w wyspecjalizowanych tablicach chemicznych).
- W ogólności zaokrąglanie masy atomowej z maturalnego Układu Okresowego (średniej ważonej średniego składu izotopowego) do liczby naturalnej, nie ma fizycznego sensu. Otrzymujesz jakąś tam, nic nieznaczącą liczbę naturalną, której nie można interpretować jako liczby masowej. Pierwszy, lepszy przykład: naturalny brom występuje w przyrodzie w formie dwóch izotopów 79Br oraz 81Br. Średnia ważona średniego składu izotopowego, czyli kolokwialnie mówiąc, masa atomowa bromu wpisana do maturalnego Układu Okresowego wynosi: M = 79,90 u. Zaokrąglenie tej wartości zgodnie z regułami matematyki daje wartość 80, która nie jest żadną z liczb masowych żadnego z dwóch izotopów występujących w przyrodzie!
- Jeśli masz wiedzę, że dany pierwiastek jest tzw. pierwiastkiem mononuklidowym (np. informacja wstępna z zadania, inne źródła danych), to wtedy matematyczne zaokrąglenie podanej w Układzie Okresowym masy atomowej daje liczbę naturalną będącą wyjątkowo liczbą masową jednego, jedynego nuklidu danego pierwiastka mononuklidowego, np.
MNa = 23,00 u => A = 23 => jedyny, naturalny nuklid: 23Na
MAl = 26,98 u => A = 27 => jedyny, naturalny nuklid: 27Al
MF = 19,00 u => A = 19 => jedyny, naturalny nuklid: 19F …itd.
Powyższa zasada nie działa w przeciwnym kierunku, tzn. jeśli masa atomowa jakiegoś pierwiastka w Układzie Okresowym jest liczbą bardzo zbliżoną do liczby naturalnej, to ten pierwiastek jest mononuklidowy !
Wyjaśnienie poniżej:
Definicja: Pierwiastek mononuklidowy to pierwiastek, który występuje w przyrodzie (czy to w wolnej postaci, czy w formie związków chemicznych) w postaci TYLKO JEDNEGO, JEDYNEGO NUKLIDU O ŚCIŚLE OKREŚLONEJ LICZBIE MASOWEJ.
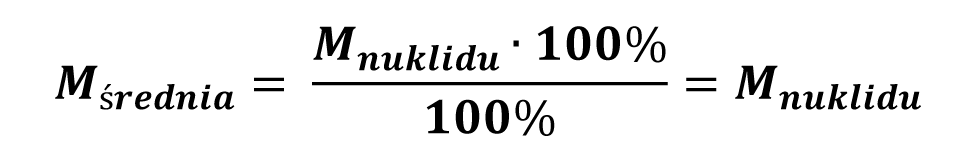
Dodatkowo stosując maturalne uproszczenie, pomijające masę elektronów i efekt związany z defektem masy mamy:

Stąd otrzymujemy, dlaczego dla pierwiastków mononuklidowych tak można robić, a dla nie mononuklidowych nie.[/vc_column_text][/vc_column][/vc_row][vc_row][vc_column][vc_column_text]Proszę Cytować jako: W. Grzesiak, „Z serii obalamy szkolne mity – liczby masowe można odczytać z układu okresowego?”, https://chemiadlamaturzysty.pl/z-serii-obalamy-szkolne-mity-liczby-masowe-mozna-odczytac-z-ukladu-okresowego/[/vc_column_text][/vc_column][/vc_row]
